
一、產品概述
(一)產品結構及組成
放射性粒籽植入專用穿刺針由針管、針座、襯芯、襯芯座及限位環組成。
(二)產品適用范圍
配合放射性粒籽防護植入器使用,將放射性粒籽植入至腫瘤靶向位置,用于腫瘤介入內放療。
(三)型號/規格
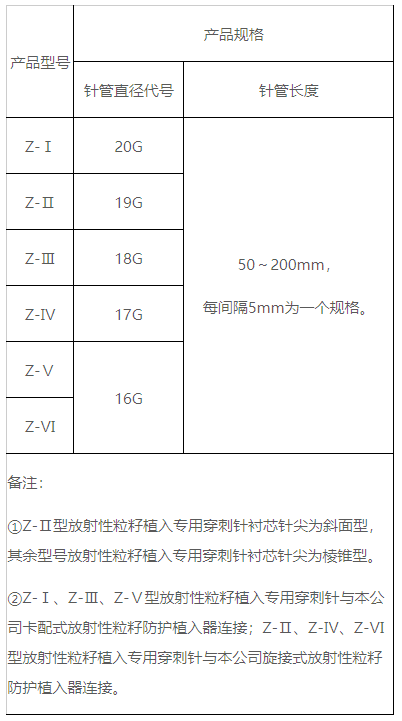
(四)工作原理
放射性粒籽植入專用穿刺針配合放射性粒籽防護植入器,將放射性粒籽植入至腫瘤靶向位置。放射性粒籽植入專用穿刺針在影像設備引導下,利用襯芯進行穿刺、導向,在植入靶點定位正確后拔出襯芯,使針管形成粒籽植入通道,針座用來連接放射性粒籽防護植入器。
二、臨床前研究概述
(一)產品性能研究
該產品性能指標包括針管剛性、針管韌性、針管耐腐蝕性、連接牢固度、微粒污染、重要部位尺寸、配合性能、化學性能、環氧乙烷殘留量、細菌內毒素等。
申請人針對上述性能指標進行了檢測,提供了天津醫療器械檢測所的檢測報告,被檢產品符合產品技術要求。
(二)生物相容性
該產品為外部接入器械,接觸部位為組織/骨,接觸時間為短期接觸。
申請人依據GB/T 16886系列標準進行了生物相容性評價,提供了細胞毒性、皮膚致敏、皮內反應、急性全身毒性和熱原試驗報告,生物相容性風險可接受。
(三)滅菌
該產品采用環氧乙烷滅菌,無菌狀態提供。申請人提供了環氧乙烷滅菌確認報告,證明無菌保證水平為10-6。
(四)產品有效期和包裝
產品有效期為3年,申請人提供了3年加速老化試驗報告。申請人對產品的包裝方式進行了規定并提供了驗證報告。驗證試驗主要為無菌包裝封口過程確認報告、產品包裝運輸驗證報告等,包裝完整性符合設計要求。
三、臨床評價概述
申請人采用同品種比對路徑開展臨床評價。按照《醫療器械臨床評價技術指導原則》要求提交了臨床評價資料,證明申報產品與同品種醫療器械基本等同,二者差異不會對申報產品的安全有效性產生不利影響。
申請人申請境內第三類醫療器械產品注冊,該產品為境內同品種首個醫療器械,注冊申報資料齊全,符合要求。
依據《醫療器械監督管理條例(國務院令第 680?號)、《醫療器械注冊管理辦法》(國家食品藥品監督管理總局令 2014年第 4 號)等相關醫療器械法規及配套規章,技術審評經系統評價產品安全性和有效性后,基于當前認知水平,認為該產品受益大于風險,注冊申報資料符合現行技術審評要求,建議予以注冊。