
11月23日,國(guó)家藥品監(jiān)督管理局就《醫(yī)療器械不良事件監(jiān)測(cè)和再評(píng)價(jià)管理辦法(修正案草案)》(以下簡(jiǎn)稱《辦法》)公開征求意見。
醫(yī)療器械不良事件監(jiān)測(cè)是實(shí)施醫(yī)療器械上市后監(jiān)管的重要工作內(nèi)容,是強(qiáng)化醫(yī)療器械全生命周期監(jiān)管、實(shí)現(xiàn)科學(xué)監(jiān)管、提高監(jiān)管成效的重要舉措。
2021年6月1日,新修訂版《醫(yī)療器械監(jiān)督管理?xiàng)l例》正式施行。《條例》結(jié)合監(jiān)管實(shí)際,提出醫(yī)療器械“注冊(cè)人、備案人”概念,對(duì)應(yīng)上市許可持有人概念。現(xiàn)國(guó)家藥監(jiān)局結(jié)合《條例》的修訂內(nèi)容,對(duì)《醫(yī)療器械不良事件監(jiān)測(cè)和再評(píng)價(jià)管理辦法》進(jìn)行了局部修改,主要涉及全面實(shí)施醫(yī)療器械注冊(cè)人制度,修改相關(guān)名詞表述,調(diào)整個(gè)別監(jiān)管措施,修改相關(guān)罰則表述。
醫(yī)療器械不良事件是指已上市的醫(yī)療器械,在正常使用情況下發(fā)生的、導(dǎo)致或者可能導(dǎo)致人體傷害的各種有害事件。報(bào)告醫(yī)療器械不良事件應(yīng)當(dāng)遵循可疑即報(bào)的原則,即懷疑某事件為醫(yī)療器械不良事件時(shí),均可以作為醫(yī)療器械不良事件進(jìn)行報(bào)告。
近年來,醫(yī)療器械不良事件時(shí)有發(fā)生。2020年,國(guó)家醫(yī)療器械不良事件監(jiān)測(cè)信息系統(tǒng)收到醫(yī)療器械不良事件報(bào)告536,055份,比上年增加35.25%。

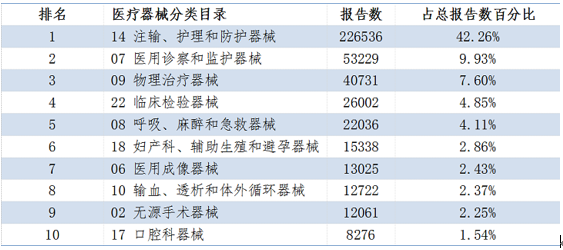
2020年醫(yī)療器械不良事件報(bào)告涉及醫(yī)療器械分類目錄情況,圖源:國(guó)家藥監(jiān)局
近年來,我國(guó)對(duì)醫(yī)療器械上市后監(jiān)管及臨床使用安全越加重視,醫(yī)療器械不良事件監(jiān)測(cè)和再評(píng)價(jià)作為醫(yī)療器械上市后監(jiān)管體系中的重要環(huán)節(jié)也將面臨更加嚴(yán)苛的監(jiān)管。對(duì)于醫(yī)療器械的各個(gè)參與方亦應(yīng)該及時(shí)了解、遵循相關(guān)法律法規(guī)。